贾丹兵,朱 宇,刘 珊,李乃民,唐立明,张永丰,王正雷,孙旗立
(解放军第211医院药剂科,黑龙江哈尔滨150080)
【摘 要】 目的: 建立双抗体夹心ABC-ELISA法,研究红光照射对创伤愈合的作用机制。 方法: 40 名受使者随机分为4组,每组10人, A组: 20 mW / cm2 ; B 组: 30 mW / cm2 ; C组: 40mW / cm2 ;D组:对照组。 红光照射45 min /次, 1次/d,连续10d,采用双抗体夹心ABC-EL ISA 法测定受试者VEGF, PDGF,TGF-β1, bFGF含量变化情况。 结果: 双抗体夹心ABC-EL ISA法检测VEGF, PDGF, TGF-β1, bFGF具有很好的特异性,红光照射组VEGF, PDGF, TGF-β1, bFGF 含量高于对照组( P<0.05) ,在30 mW / cm2 红光照射时, bFGF含量最高。 结论: 红光照射加快创伤愈合与促进VEGF, PDGF, TGF-β1, bFGF分泌有关,有利于临床推广应用。
【关键词】红光;创伤愈合;双抗体夹心法;酶联免疫吸附实验
引 言
红光是指波长600~700 nm,可以对生物体产生光化学作用的光线。 红光可直接作用于血管、淋巴管、神经末梢和皮下组织等而发挥着相应的治疗作用。 近年来有关红光的临床研究正越来越多被人们认识和重视。 Reddy等[1]应用红光照射糖尿病小鼠的实验研究中发现, 632 nm的红光可以使照射组小鼠的伤口愈合强度、拉力、负重力和坚韧度比对照组明显提高,总胶原浓度也明显升高。 Schindl等[2]应用红光照射不同原因导致的难治性溃疡患者,所有患者的溃疡在足够的照射后均能愈合,且无明显毒副作用。 我们采用双抗体夹心法(ABC-ELISA)测定了红光照射对40 名志愿者血管内皮细胞生长因子(VEGF) ,血小板衍生生长因子( PDGF) ,转化生长因子( TGF-β1) ,碱性成纤维细胞生长因子( bFGF)含量的影响,进一步从分子生物学角度证实红光对软组织创伤及伤口愈合的影响,为红光照射治疗软组织创伤及伤口愈合适应症提供了理论依据。
材料和方法
材料 2006209 /2007208 选取本院40 名志愿者,无光过敏史及近期服用光过敏剂者;无慢性溶血,出凝血功能异常者和无明显出血倾向者及卟啉病者。将40名志愿者随机分为4组,每组10人。 A 组: 20mW / cm2 ; B组:30 mW / cm2 ; C组:40 mW / cm2 ; D组:对照组。 红光照射组照射1次/d,每次45 min, 10次,对照组用日光灯照射,照射时间、次数和实验组相同。VEGF,PDGF,TGF-β1,bFGF标准品和单克隆抗体,生物素标记的VEGF,PDGF,TGF-β1, bFGF单抗均由本实验室制备;辣根过氧化物酶标记Strep tavidin (华美生物技术有限公司);预包被的96孔微孔检测板( Pierce公司) ;显色酶底物OPD ( Sigma公司) ,紫外分光光度计(Amersham公司),680型酶标仪(B ioRad公司),HG-675型红光治疗机(深圳一体智能技术有限公司),受试人血样40份。
方法 样本采集 受试者采集全血5mL,不加抗凝剂,直接分离血清,放置- 20℃冰箱备用。VEGF, PDGF,TGF-β1,bFGF含量的测定将450μL样本稀释液加入到1.5mL进口聚丙烯管中,再加入10μL血清样本,加入20μL (1 mol/L) HCL,2~ 8℃放置60 min,后再加入20 μL ( 1 mol/L )NaOH,上下混匀既用或放置- 20℃冰箱备用。 单克隆抗体的生物素化标记方法,参照常规方法[4-5] 。 双抗体夹心
ABC2EL ISA法测定VEGF, PDGF, TGF-β1,bFGF含量,在配置好的标准溶液中各加入25μL待测试样品,充分混匀,37℃孵育30min,洗涤液洗涤;加入生物素化抗体50 μL,充分混匀,37℃孵育30min,洗涤液洗涤;加入辣根过氧化物酶标记Strep tavidin液100μL,充分混匀,37℃孵育60 min,洗涤;后再加入酶底物OPD 100 μL,37℃暗处反应5~10min,使底物显色;最后加入2 mol/L硫酸50μL,终止反应。在BioRad680型酶标仪上测量吸光度(A492 nm )值。
统计学处理: 计量数据以![]() ±s 表示, 应用SPSS11.0统计软件进行统计学分析,统计方法采用方差分析及Dunnett-t检验。
±s 表示, 应用SPSS11.0统计软件进行统计学分析,统计方法采用方差分析及Dunnett-t检验。
结 果
ABC-EL ISA法标准曲线的建立 以制备的各生长因子标准浓度为横坐标,以吸光度(A492 nm )值为纵坐标作图【图1】 ,当VEGF (系列1)浓度为32 ~2000 pg/mL, bFGF (系列3)浓度为16~500 pg/mL之间时,检测生长因子的浓度与其吸光度(A492 nm )值之间线性关系良好。 进行回归分析,建立ABC-EL ISA法测定生长因子的标准曲线【图2】并得到直线回归方程y = 0.34x – 0.27,当待测品在以上各浓度范围时,对数和吸光度(A492 nm )值呈线性关系。
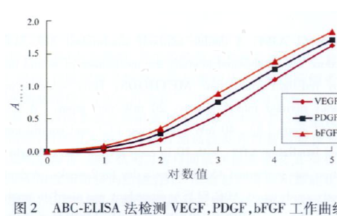
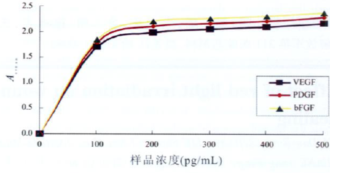
灵敏度和稳定性实验 在上述各浓度范围内,VEGF, PDGF, TGF-β1, bFGF检测限分别为50, 15.6,32, 16 pg/mL,选择生长因子不同浓度重复测定,得出批内差异分别为3.96% , 6.28% , 7. 29% , 6.83%。
特异性检测 用建立的ABC-EL ISA法测定,吸光度(A492 nm )值与阴性值接近,表明该法检测生长因子具有很好的特异性。
红光照射人体VEGF, PDGF, TGF-β1, bFGF含量比较 根据各样品A492 nm值在标准曲线上分别计算出相应人体VEGF, PDGF, TGF-β1, bFGF 的含量,其中TGF-β1实际浓度( ng) =测量浓度×稀释倍数50 /1000,数据表明红光照射组(A,B, C组)VEGF,PDGF, TGF-β1, bFGF的含量与随机对照组(D组)存在统计学差异, TGF-β1在照射剂量为30 mW / cm2 作用时分泌较其他剂量组明显【表1】。
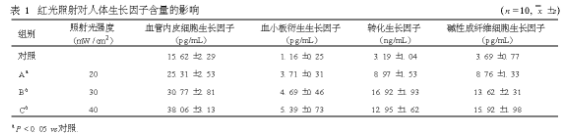
讨 论
红光是指通过物理学方法,将大部分其他光线滤去,包括滤去对皮肤有损害作用的紫外线和具有明显热效应的红外线部分,仅保留600 ~700 nm波段的光。 红光对人体穿透性较强,穿透深度可达30 mm以上,可以作为一种局部或全身的治疗手段应用于临床,发挥其多种生物学效应[6] 。 动物试验证明,红光照射可增强实验动物线粒体过氧化氢酶活性,提高细胞新陈代谢水平,使糖原、蛋白生物合成增加,促进细胞合成和伤口愈合[1] 。创伤性疾病与受损伤部位血管数量减少密切相关,创伤部位血管修复是一个复杂的生理过程,它是由许多细胞因子及生长因子通过直接或间接方式调节支配,其中血管内皮细胞生长因子(VEGF)是一种最直接的促进血管生成的多功能的细胞因子,其作用贯穿创伤组织再生修复的病理生理过程,同时VEGF是多种细胞因子诱导创伤血管生成的重要中介因子[7] 。 实验表明:与对照组相比,红光照射后血管内皮细胞生长因子(VEGF) , 血小板衍生生长因子( PDGF) ,转化生长因子( TGF-β1)分泌明显增加,并且与红光照射剂量呈现一定剂量依赖关系,即随照射剂量增加而增强,进一步表明PDGF, TGF-β1可以通过促进VEGF的分泌合成,间接加速创伤组织血管内皮细胞增值,对血管生成和创伤修复至关重要。体外实验证明,人体碱性成纤维细胞生长因子( bFGF)本身既是强有力的血管生成刺激剂,又是细胞迁移和增值的调节剂, bFGF具有促进创伤部位血管生成和早期肉芽组织形成等多种生物学效应,同时bFGF又是成纤维细胞内皮细胞强大的促分裂原和趋化因子[7 – 8] ,对人体VEGF的表达有明显的促进作用,成纤维细胞是参与伤口上皮化和愈合的重要细胞,实验发现红光照射后bFGF与对照组相比分泌明显增加,并且红光照射剂量与bFGF分泌呈非线性关系,在照射剂量为30 mW / cm2 作用时较明显,表明红光照射加快创伤愈合与促进bFGF分泌增加密切相关。实验过程中未见红光受试者出现明显不良反应,说明了红光照射对于人体无明显毒副作用,值得临床推广应用。
【参考文献】
[1] Reddy GK, Stehno2Bittel L, Enwemeka CS.Laser photo stimulation accelerateswound healing in diabetic rats [J]. Wound Repair Regen, 2001, 9: 248 - 255.
[2] SchindlM, Kerschan K, Schindl A, et al. Induction of comp lete wound healing in recalcitrant ulcers by low2intensity irradiation depends on ulcer cause and size [J]. Photoimmunol Photomed, 1999,15: 18 - 21.
[3] 贾丹民,李乃民,唐立民,等. 红光照射对人体抗疲劳能力的影响[J]. 解放军医学杂志, 2007, 32 (10) : 1086 - 1088.
[4] 李成文. 现代免疫化学技术[M]. 上海:上海科学技术出版社,1990: 79 - 101.
[5] 徐宜. 免疫检测技术[M]. 北京: 科学技术出版社, 1997:271 - 289.
[6] Yaakobi T, Maltz L, Oron U. Promotion of bone repair in the cortical bone of the tibia in rats by low energy laser (He2Ne) irradiation[J]. Calcif Tissue Int, 1996, 59: 297 - 300.
[7] Schindl A, SchindlM, Schon P, et al. Red light laser therapy: A review[J]. InvestMed, 2000, 48 (3) : 312 - 326.
[8] SchindlA, Merwald H, Schind L, et al. Direct stimulatory effect of low2intensity 670 nm laser irradiation on human endothelial cell p roliferation[J]. BrDermatol, 2003, 148: 334 - 336.
(摘自:第四军医大学学报(J FourthMilMed Univ)



